
肥満症薬「ウゴービ」11月22日に薬価収載(2023年11月15日)
中医協総会は11月15日、ウゴービ皮下注を含む13成分・35品目の新薬(下表)の薬価収載を了承した。収載日は11月22日、告示日は11月21日の予定。
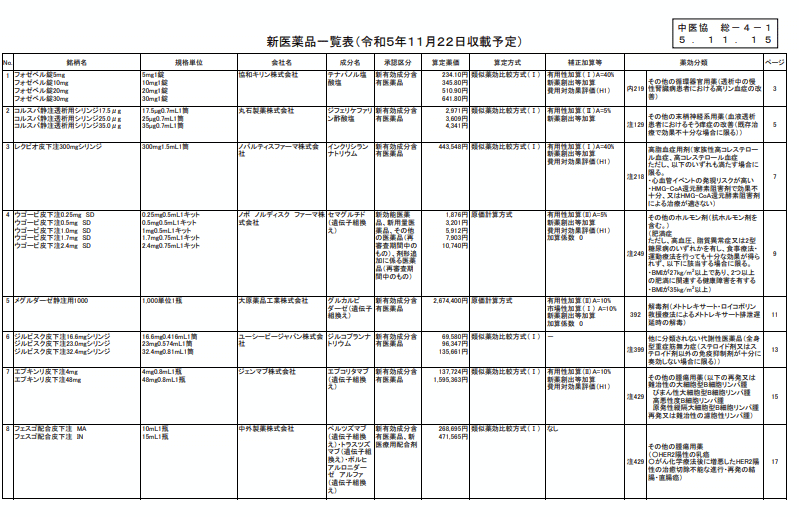
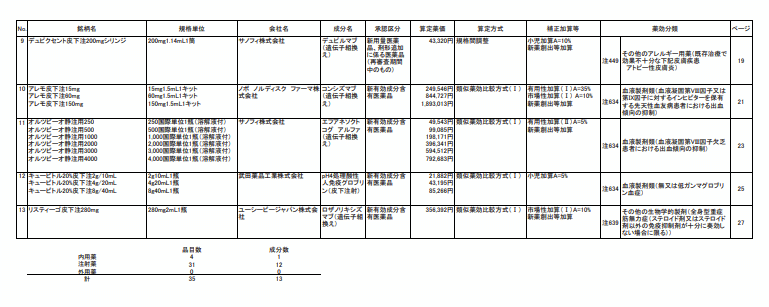
ウゴービは最適使用推進ガイドライン満たす施設のみで使用
ウゴービ(成分名:セマグルチド(遺伝子組換え))は、肥満症の適応で承認されたGLP-1受容体作動薬。
委員からは、ウゴービと同一企業(ノボノルディスクファーマ株式会社)で同一成分の糖尿病治療剤「オゼンピック」の出荷制限等を踏まえ、ウゴービに対する安定供給に懸念の声が寄せられた。
厚生労働省の薬剤管理官はこれに対し、企業側からはどの規格の製剤でも国内需要に対応可能な供給量を確保できている旨の報告を受けていると回答。オゼンピック皮下注は、現在供給制限となっており供給不足であるが、増産体制に目処が立ち、「年明けには供給制限が解除される見込み」である旨を報告した。
なお、GLP-1受容体作動薬であるオゼンピックは2型糖尿病を適応とするが、痩身・ダイエット目的の適応外使用が指摘されている。
2型糖尿病を適応とするGLP-1受容体作動薬を2型糖尿病の治療以外の目的で使用していることが明らかな場合は、適応外使用として、査定の対象
また、厚生労働省はウゴービについて、「企業側は保険診療、自由診療問わず、最適使用推進ガイドラインを満たす施設で使うことを想定した流通を考えている」旨を示した。これにより、「適切な施設への販売」を行っていくとしている。
ウゴービの「効能・効果」、「主な用法・用量」は以下の通りとなっている。
【効能・効果】
肥満症。ただし、高血圧、脂質異常症または2型糖尿病のいずれかを有し、食事療法・運動療法を行っても十分な効果が得られず、以下に該当する場合に限る。
・BMIが27㎏/㎡以上であり、2つ以上の肥満に関連する健康障害を有する
・BMIが35㎏/㎡以上
【主な用法・用量】
通常、成人には、セマグルチド(遺伝子組換え)として0.25mgから投与を開始し、週1回皮下注射する。その後は4週間の間隔で、週1回0.5mg、1.0mg、1.7mgおよび2.4mgの順に増量し、以降は2.4mgを週1回皮下注射する。なお、患者の状態に応じて適宜減量する。
レクビオ皮下注300mgシリンジについても最適使用推進ガイドラインを作成
11月22日に薬価収載予定の新薬のうち、ウゴービ皮下注以外では、レクビオ皮下注300mgシリンジ(インクリシランナトリウム)についても、最適使用推進ガイドラインが作成される。
最適使用推進ガイドライン作成に伴い、ウゴービとレクビオにおける診療報酬明細書(レセプト)の摘要欄に記載を求める事項は以下の通りとなる予定。
ウゴービ
①医療施設の要件への該当性
②治療の責任者の要件への該当性
③投与対象となる患者要件への該当性
④投与継続の判断レクビオ
①治療の責任者の要件への該当性
②投与対象となる患者要件への該当性
③投与継続の判断
なお、以下の❶・❷の品目に係る最適使用推進ガイドラインの改訂に伴い、保険適用上の留意事項も変更となる予定。
❶レパーサ皮下注140mgペン、レパーサ皮下注420mgオートミニドーザー
❷デュピクセント皮下注300mgペン、デュピクセント皮下注300mgシリンジ、デュピクセント皮下注200mgシリンジ

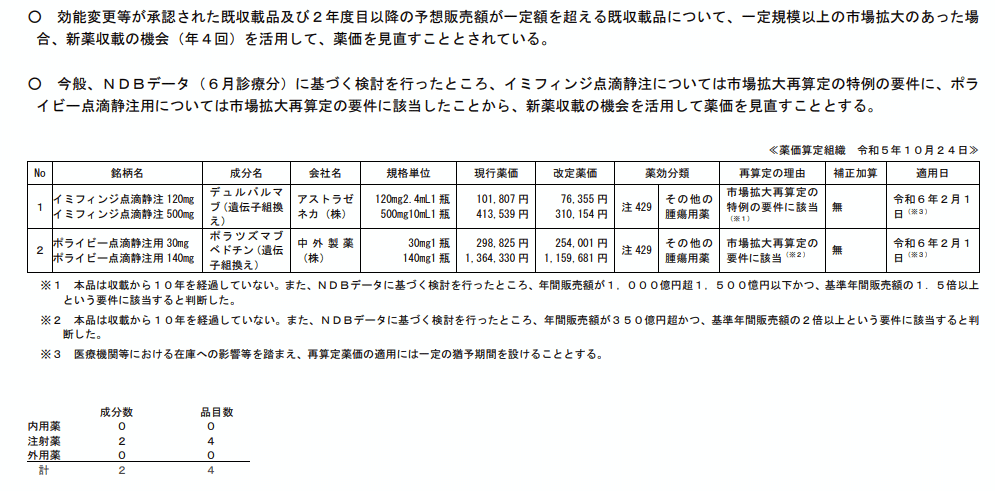
イミフィンジ、ポライビーは市場拡大再算定で薬価改定
11月15日の中医協総会では、イミフィンジ点滴静注120mg・同500m(デュルバルマブ)、ポライビー点滴静注用30mg・同140mg(ポラツズマブベドチン)の市場拡大再算定による薬価見直しについても了承された。
適用日は令和6年2月1日となっている。
レットヴィモ、ウィフガート、ジスバルは費用対効果評価で価格調整
そのほか、レットヴィモカプセル40mg・同80mg(セルペルカチニブ)、ウィフガート点滴静注400mg(エフガルチギモド アルファ)、ジスバルカプセル40mg(バルベナジントシル酸塩)については、費用対効果評価結果に基づき薬価の価格調整が行われる。
適用日は令和6年2月1日。
新薬のジルビスク、アレモは在宅自己注の対象に
11月22日に薬価収載予定の新薬のうち、ジルビスク皮下注16.6mgシリンジ・同23.0mgシリンジ・同32.4mgシリンジ(ジルコプランナトリウム)、アレモ皮下注15㎎・同60㎎・同150㎎(コンシズマブ)については、「保険医が投与することができる注射薬(処方箋を交付することができる注射薬)」および「在宅自己注射指導管理料の対象薬剤」として追加することも了承された。
ジルビスクおよびアレモの「効能・効果」、「主な用法・用量」は以下の通りとなっている。
【ジルビスクの効能・効果】
全身型重症筋無力症(ステロイド剤またはステロイド剤以外の免疫抑制剤が十分に奏効しない場合に限る)
【ジルビスクの主な用法・用量】
通常、成人にはジルコプランとして下表に示す用量を1日1回皮下投与する。
体重 | 投与量
------ | --------
56kg未満 | 16.6mg
56kg以上77kg未満 | 23.0mg
77kg以上 | 32.4mg
【アレモの効能・効果】
血液凝固第Ⅷ因子又は第Ⅸ因子に対するインヒビターを保有する先天性血友病患者における出血傾向の抑制
【アレモの主な用法・用量】
通常、12歳以上の患者には、1日目に負荷投与としてコンシズマブ(遺伝子組換え)1mg/kgを皮下投与する。2日目以降は維持用量として1日1回、0.20mg/kgを皮下投与する。なお、0.20mg/kgの投与を開始後、コンシズマブの血中濃度や患者の状態により、0.15mg/kgに減量または0.25mg/kgに増量できる。
なお、バイオ後続品のアダリムマブ(遺伝子組換え)[アダリムマブ後続4]については、先行品(ヒュミラ)と比較して、効能・効果や用法・用量等は同等であり、先行品の使用状況等にも特段の問題はないことから、在宅自己注射指導管理料の対象薬剤に追加されることが了承された。



